Химические соединения, которые состоят в том числе и из карбоксильной группы COOH, получили от ученых название карбоновые кислоты. Существует большое количество наименований этих соединений. Они классифицируются по разным параметрам, например, по количеству функциональных групп, наличию ароматического кольца и так далее.
Строение карбоновых кислот
Как уже упоминалось, для того чтобы кислота была карбоновой, она должна иметь карбоксильную группу, которая, в свою очередь, имеет две функциональные части: гидроксил и карбонил. Их взаимодействие обеспечивается ее функциональным сочетанием одного атома углерода с двумя кислородными. Химические свойства карбоновых кислот зависят от того, какое строение имеет эта группа.
За счет карбоксильной группы эти органические соединения можно называть кислотами. Их свойства обуславливаются повышенной способностью иона водорода H+ притягиваться к кислороду, дополнительно поляризуя связь O-H. Также благодаря этому свойству органические кислоты способны диссоциировать в водных растворах. Способность к растворению уменьшается обратно пропорционально росту молекулярной массы кислоты.
Разновидности карбоновых кислот
Химики выделяют несколько групп органических кислот.
Моноосновные карбоновые кислоты состоят из углеродного скелета и только одной функциональной карбоксильной группы. Каждый школьник знает химические свойства карбоновых кислот. 10 класс учебной программы по химии включает в себя непосредственно изучение свойств одноосновных кислот. Двухосновные и многоосновные кислоты имеют в своей структуре две и более карбоксильных групп соответственно.

Также по наличию или отсутствию двойных и тройных связей в молекуле бывают ненасыщенные и насыщенные карбоновые кислоты. Химические свойства и их отличия будут рассмотрены ниже.
Если органическая кислота имеет в составе радикала замещенный атом, то в ее название включается наименование группы-заместителя. Так, если атом водорода замещен галогеном, то в названии кислоты будет присутствовать наименование галогена. Такие же изменения претерпит наименование, если произойдет замещение на альдегидную, гидроксильную или аминогруппы.
Изомерия органических карбоновых кислот
В основе получения мыла лежит реакция синтеза сложных эфиров вышеперечисленных кислот с калиевой или натриевой солью.
Способы получения карбоновых кислот
Способов и методов получения кислот с группой COOH существует множество, но наиболее часто применяются следующие:
- Выделение из природных веществ (жиров и прочего).
- Окисление моноспиртов или соединений с COH-группой (альдегидов): ROH (RCOH) [O] R-COOH.
- Гидролиз тригалогеналканов в щелочи с промежуточным получением моноспирта: RCl3 +NaOH=(ROH+3NaCl)=RCOOH+H2O.
- Омыление или гидролиз эфиров кислоты и спирта (сложных эфиров): R−COOR"+NaOH=(R−COONa+R"OH)=R−COOH+NaCl.
- Окисление алканов перманганатом (жесткое окисление): R=CH2 [O], (KMnO4) RCOOH.
Значение карбоновых кислот для человека и промышленности

Химические свойства карбоновых кислот имеют большое значение для жизнедеятельности человека. Они чрезвычайно необходимы для организма, так как в большом количестве содержатся в каждой клетке. Метаболизм жиров, белков и углеводов всегда проходит через стадию, на которой получается та или иная карбоновая кислота.
Кроме того, карбоновые кислоты используют при создании лекарственных препаратов. Ни одна фармацевтическая промышленность не может существовать без применения на деле свойств органических кислот.

Немаловажную роль соединения с карбоксильной группой играют и в косметической промышленности. Синтез жира для последующего изготовления мыла, моющих средств и бытовой химии основан на реакции этерификации с карбоновой кислотой.
Химические свойства карбоновых кислот находят отражение в жизнедеятельности человека. Они имеют большое значение для человеческого организма, так как в большом количестве содержатся в каждой клетке. Метаболизм жиров, белков и углеводов всегда проходит через стадию, на которой получается та или иная карбоновая кислота.
Образование галогеналканов при взаимодействии спиртов с галогеноводородами - обратимая реакция. Поэтому понятно, что спирты могут быть получены при гидролизе галогеналканов - реакции этих соединений с водой:
Многоатомные спирты можно получить при гидролизе галогеналканов, содержащих более одного атома галогена в молекуле. Например:
Гидратация алкенов
Гидратация алкенов - присоединение воды по π — связи молекулы алкена, например:
![]()
Гидратация пропена приводит в соответствии с правилом Марковникова к образованию вторичного спирта - пропанола-2:

Гидрирование альдегидов и кетонов
Окисление спиртов в мягких условиях приводит к образованию альдегидов или кетонов. Очевидно, что спирты могут быть получены при гидрировании (восстановлении водородом, присоединении водорода) альдегидов и кетонов:

Окисление алкенов
Гликоли, как уже отмечалось, могут быть получены при окислении алкенов водным раствором перманганата калия. Например, этиленгликоль (этандиол-1,2) образуется при окислении этилена (этена):
Специфические способы получения спиртов
1. Некоторые спирты получают характерными только для них способами. Так, метанол в промышленности получают реакцией взаимодействия водорода с оксидом углерода (II) (угарным газом) при повышенном давлении и высокой температуре на поверхности катализатора (оксида цинка):
![]()
Необходимую для этой реакции смесь угарного газа и водорода, называемую также «синтез-газ», получают при пропускании паров воды над раскаленным углем:
![]()
2. Брожение глюкозы . Этот способ получения этилового (винного) спирта известен человеку с древнейших времен:
![]()
Основными способами получения кислородсодержащих соединений (спиртов) являются: гидролиз галогеналканов, гидратация алкенов, гидрирование альдегидов и кетонов, окисление алкенов, а также получение метанола из «синтез-газа» и сбраживание сахаристых веществ.
Способы получения альдегидов и кетонов
1. Альдегиды и кетоны могут быть получены окислением или дегидрированием спиртов . При окислении или дегидрировании первичных спиртов могут быть получены альдегиды, а вторичных спиртов - кетоны:
 3CH 3 –CH 2 OH + K 2 Cr 2 O 7 + 4H 2 SO 4 = 3CH 3 –CHO + K 2 SO 4 + Cr 2 (SO 4) 3 + 7H 2 O
3CH 3 –CH 2 OH + K 2 Cr 2 O 7 + 4H 2 SO 4 = 3CH 3 –CHO + K 2 SO 4 + Cr 2 (SO 4) 3 + 7H 2 O
2. Реакция Кучерова. Из ацетилена в результате реакции получается уксусный альдегид, из гомологов ацетилена - кетоны:

3. При нагревании кальциевых или бариевых солей карбоновых кислот образуются кетон и карбонат металла:

Способы получения карбоновых кислот
1. Карбоновые кислоты могут быть получены окислением первичных спиртов или альдегидов :
 3CH 3 –CH 2 OH + 2K 2 Cr 2 O 7 + 8H 2 SO 4 = 3CH 3 –COOH + 2K 2 SO 4 + 2Cr 2 (SO 4) 3 + 11H 2 O
3CH 3 –CH 2 OH + 2K 2 Cr 2 O 7 + 8H 2 SO 4 = 3CH 3 –COOH + 2K 2 SO 4 + 2Cr 2 (SO 4) 3 + 11H 2 O
5CH 3 –CHO + 2KMnO 4 + 3H 2 SO 4 =5CH 3 –COOH + 2MnSO 4 + K 2 SO 4 + 3H 2 O,
3CH 3 –CHO + K 2 Cr 2 O 7 + 4H 2 SO 4 = 3CH 3 –COOH + Cr 2 (SO 4) 3 + K 2 SO 4 + 4H 2 O,
CH 3 –CHO + 2OH CH 3 –COONH 4 + 2Ag + 3NH 3 + H 2 O.
Но при окислении метаналя аммиачным раствором оксида серебра, образуется карбонат аммония, а не муравьиная кислота:
HCHО + 4OH = (NH 4) 2 CO 3 + 4Ag + 6NH 3 + 2H 2 O.
2. Ароматические карбоновые кислоты образуются при окислении гомологов бензола :

5C 6 H 5 –CH 3 + 6KMnO 4 + 9H 2 SO 4 = 5C 6 H 5 COOH + 6MnSO 4 + 3K 2 SO 4 + 14H 2 O,
5C 6 H 5 –C 2 H 5 + 12KMnO 4 + 18H 2 SO 4 = 5C 6 H 5 COOH + 5CO 2 + 12MnSO 4 + 6K 2 SO 4 + 28H 2 O,
C 6 H 5 –CH 3 + 2KMnO 4 = C 6 H 5 COOK + 2MnO 2 + KOH + H 2 O
3. Гидролиз различных производных карбоновых кислот также приводит к получению кислот. Так, при гидролизе сложного эфира образуются спирт и карбоновая кислота. Реакции этерификации и гидролиза, катализируемой кислотой, обратимы:
4. Гидролиз сложного эфира под действием водного раствора щелочи протекает необратимо, в этом случае из сложного эфира образуется не кислота, а ее соль.
Химические соединения, основу которых составляет одна и более групп СООН, получили определение карбоновые кислоты.
В основу соединений входит группа СООН, имеющая два составляющих — карбонил и гидроксил. Группу атомов СООН называют карбоксильной группой (карбоксилом). Взаимодействие элементов обеспечивается сочетанием двух атомов кислорода и атома углерода.
Вконтакте
Строение карбоновых кислот
Углеводородный радикал в одноосновных предельных кислотах соединяется с одной группой СООН. Общая формула карбоновых кислот выглядит так: R-COOH.
Строение карбоновой группы влияет на химические свойства.
Номенклатура
В названии карбоновых соединений сначала нумеруют атом углерода группы COOH. Количество карбоксильных групп обозначают приставками ди-; три-; тетра-.
Например,СН3-СН2-СООН — формула пропановой кислоты.
У карбоновых соединений существуют и привычные слуху названия: муравьиная, уксусная, лимонная…Все это названия карбоновых кислот.
Названия солей карбоновых соединений получаются из названий углеводорода с добавлением суффикса «-оат» (СООК)2- этандиот калия.
Классификация карбоновых кислот
Карбоновые кислоты классификация .
По характеру углеводорода:
- предельные;
- непредельные;
- ароматические.
По количеству групп СООН бывают:
- одноосновные (уксусная кислота);
- двуосновные (щавелевая кислота);
- многоосновные (лимонная кислота).
Предельные карбоновые кислоты — соединения, в которых радикал соединен с одним карбонилом.
Классификация карбоновых кислот разделяет их еще и по строению радикала, с которым связан карбонил. По этому признаку соединения бывают алифатические и алициклические.
Физические свойства
 Рассмотрим карбоновые кислоты физические свойства.
Рассмотрим карбоновые кислоты физические свойства.
Карбоновые соединения имеют различное число атомов углерода. В зависимости от этого числа физические свойства этих соединений различаются.
Соединения, имеющие в составе от одного до трех углеродных атомов, считаются низшими. Это жидкости без цвета с резким запахом. Низшие соединения с легкостью растворяются в воде.
Соединения, имеющие в составе от четырех до девяти углеродных атомов — маслянистые жидкости, имеющие неприятный запах.
Соединения, имеющие в составе более девяти углеродных атомов, считаются высшими и физические свойства этих соединений таковы: они являются твердыми веществами , их невозможно растворить в воде.
Температура кипения и плавления зависит от молекулярной массы вещества. Чем больше молекулярная масса, тем выше температура кипения. Для закипания и плавления нужна более высокая температура, чем спиртам.
Существует несколько способов получения карбоновых кислот .

При химических реакциях проявляются следующие свойства:

Применение карбоновых кислот
Карбоновые соединения распространены в природе.Поэтому их применяют во многих областях: в промышленности (легкой и тяжелой), в медицине и сельском хозяйстве , а также в пищевой промышленности и косметологии.
Ароматические в большом количестве содержатся в ягодах и фруктах.
В медицине используют молочную, винную и аскорбиновую кислоту. Молочную применяют в качестве прижигания, а винную — как легкое слабительное. Аскорбиновая укрепляет иммунитет.
 В косметологии используются фруктовые и ароматические. Благодаря им клетки быстрее обновляются. Аромат цитрусовых способен оказать тонизирующее и успокаивающее действие на организм. Бензойная встречается в бальзамах и эфирных маслах, она хорошо растворяется в спирте.
В косметологии используются фруктовые и ароматические. Благодаря им клетки быстрее обновляются. Аромат цитрусовых способен оказать тонизирующее и успокаивающее действие на организм. Бензойная встречается в бальзамах и эфирных маслах, она хорошо растворяется в спирте.
Высокомолекулярные непредельные соединения встречаются в диетологии. Олеиновая в этой области наиболее распространена.
Полиненасыщенные с двойными связями (линолевая и другие) обладают биологической активностью. Их еще называют активными жирными кислотами. Они участвуют в обмене веществ, влияют на зрительную функцию и иммунитет, а также на нервную систему. Отсутствие этих веществ в пище или недостаточное их употребление затормаживает рост животных и оказывает негативное влияние на их репродуктивную функцию.
Сорбиновая получается из ягод рябины. Она является отличным консервантом .
Акриловая имеет едкий запах. Она применяется для получения стекла и синтетических волокон.
На основе реакции этирификации происходит синтез жира, который применяют при изготовлении мыла, а также моющих средств.
Муравьиная используется в медицине , в пчеловодстве, а также в качестве консервантов.
Уксусная — жидкость без цвета с резким запахом; легко смешивается с водой. Ее широко применяют в пищевой промышленности в качестве приправы. Также она используется при консервации. Еще она обладает свойствами растворителя. Поэтому широко применяется в производстве лаков и красок, при крашении. На ее основе изготавливают сырье для борьбы с насекомыми и сорняками.
Стеариновая и пальмитиновая (высшие одноосновные соединения) являются твердыми веществами и не растворяются в воде. Но их соли применяются в производстве мыла. Они делают брикеты мыла твердыми.
Поскольку соединения способны придавать однородность массам, то они широко используются в изготовлении лекарств.
Растения и животные также вырабатывают карбоновые соединения. Поэтому употреблять их внутрь безопасно. Главное, — соблюдать дозировку. Превышение дозы и концентрации ведет к ожогам и отравлениям.
Едкость соединений приносит пользу в металлургии, а также реставраторам и мебельщикам. Смеси на их основе позволяют выравнивать поверхности и очищать ржавчину.
Сложные эфиры, получаемые при реакции этерификации, нашли свое применение в парфюмерии. Они используются также в качестве компонентов лаков и красок, растворителей. А также как аромадобавки.
Получение карбоновых кислот
I . В промышленности
1. Выделяют из природных продуктов
(жиров, восков, эфирных и растительных масел)
2. Окисление алканов:
2CH 4 + + 3O 2 t,kat → 2HCOOH + 2H 2 O
метан муравьиная кислота
2CH 3 -CH 2 -CH 2 -CH 3 + 5O 2 t,kat,p → 4CH 3 COOH + 2H 2 O
н-бутан уксусная кислота
3. Окисление алкенов:
CH 2 =CH 2 + O 2 t,kat → CH 3 COOH
этилен
СH 3 -CH=CH 2 + 4[O] t,kat → CH 3 COOH + HCOOH (уксусная кислота+муравьиная кислота )
4. Окисление гомологов бензола (получение бензойной кислоты):
C 6 H 5 -C n H 2n+1 + 3n[O] KMnO4,H+ → C 6 H 5 -COOH + (n-1)CO 2 + nH 2 O
5C 6 H 5 -CH 3 + 6KMnO 4 + 9H 2 SO 4 → 5C 6 H 5 -COOH + 3K 2 SO 4 + 6MnSO 4 + 14H 2 O
толуол бензойная кислота
5. Получение муравьиной кислоты:
1 стадия: CO + NaOH t , p → HCOONa ( формиат натрия – соль )
2 стадия : HCOONa + H 2 SO 4 → HCOOH + NaHSO 4
6. Получение уксусной кислоты:
CH 3 OH + CO t,p → CH 3 COOH
Метанол
II . В лаборатории
1. Гидролиз сложных эфиров:
2. Из солей карбоновых кислот :
R-COONa + HCl → R-COOH + NaCl
3. Растворением ангидридов карбоновых кислот в воде:
(R-CO) 2 O + H 2 O → 2 R-COOH
4. Щелочной гидролиз галоген производных карбоновых кислот:

III . Общие способы получения карбоновых кислот
1. Окисление альдегидов:
R-COH + [O] → R-COOH
Например, реакция «Серебряного зеркала» или окисление гидроксидом меди (II ) – качественные реакции альдегидов
2. Окисление спиртов:
R-CH 2 -OH + 2[O] t,kat → R-COOH + H 2 O
3. Гидролиз галогензамещённых углеводородов, содержащих три атома галогена у одного атома углерода.

4. Из цианидов (нитрилов) – способ позволяет наращивать углеродную цепь:
СH 3 -Br + Na-C≡N → CH 3 -CN + NaBr
CH 3 —CN — метилцианид (нитрил уксусной кислоты)
СH 3 -CN + 2H 2 O t → CH 3 COONH 4
ацетат аммония
CH 3 COONH 4 + HCl → CH 3 COOH + NH 4 Cl
5. Использование реактива Гриньяра
Карбоновыми кислотами называют производные углеводородов, содержащие одну или несколько карбоксильных групп.
Число карбоксильных групп характеризует основность кислоты.
В зависимости от количества карбоксильных групп карбоновые кислоты подразделяются на одноосновные карбоновые кислоты (содержат одну карбоксильную группу), двухосновные (содержат две карбоксильные группы) и многоосновные кислоты.
В зависимости от вида радикала, связанного с карбоксильной группой, карбоновые кислоты делятся на предельные, непредельные и ароматические. Предельные и непредельные кислоты объединяют под общим названием кислоты алифатического или жирного ряда.
Одноосновные карбоновые кислоты
1.1 Гомологический ряд и номенклатура
Гомологический ряд одноосновных предельных карбоновых кислот (иногда их называют жирными кислотами) начинается с муравьиной кислоты
Формула гомологического ряда
Номенклатура ИЮПАК разрешает сохранять для многих кислот их тривиальные названия, которые обычно указывают на природный источник, из которого была выделена та или иная кислота, например, муравьиная, уксусная, масляная, валериановая и т.д.
Для более сложных случаев названия кислот производят от названия углеводородов с тем же числом атомов углерода, что и в молекуле кислоты, с добавлением окончания -овая и слова кислота. Муравьиная кислота Н-СООН называется метановой кислотой, уксусная кислота СН 3 -СООН - этановой кислотой и т. д.
Таким образом, кислоты рассматриваются как производные углеводородов, одно звено которых превращено в карбоксил:

При составлении названий кислот с разветвленной цепью по рациональной номенклатуре их рассматривают как производные уксусной кислоты, в молекуле которой атомы водорода замещены радикалами, например, триметилуксусная кислота (СН 3) 3 С – СООН.
1.2 Физические свойства карбоновых кислот
Только с чисто формальных позиций можно рассматривать карбоксильную группу как комбинацию карбонильной и гидроксильной функций. Фактически их взаимное влияние друг на друга таково, что полностью изменяет их свойства.
Обычная для карбонила поляризация двойной связи С=0 сильно возрастает за счет дополнительного стягивания свободной электронной пары с соседнего атома кислорода гидроксильной группы:
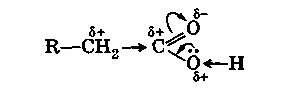
Следствием этого является значительное ослабление связи О-Н в гидроксиле и легкость отщепления атома водорода от него в виде протона (Н +). Появление пониженной электронной плотности (δ+) на центральном углеродном атоме карбоксила приводит также к стягиванию σ-электронов соседней связи С-С к карбоксильной группе и появлению (как у альдегидов и кетонов) пониженной электронной плотности (δ +) на α-углеродном атоме кислоты.
Все карбоновые кислоты обладают кислой реакцией (обнаруживается индикаторами) и образуют соли с гидроксидами, оксидами и карбонатами металлов и с активными металлами:
Карбоновые кислоты в большинстве случаев в водном растворе диссоциированы лишь в малой степени и являются слабыми кислотами, значительно уступая таким кислотам, как соляная, азотная и серная. Так, при растворении одного моля в 16 л воды степень диссоциации муравьиной кислоты равна 0,06, уксусной кислоты - 0,0167, в то время как соляная кислота при таком разбавлении диссоциирована почти полностью.
Для большинства одноосновных карбоновых кислот рК а = 4,8, только муравьиная кислота имеет меньшую величину рК а (около 3,7), что объясняется отсутствием электронодонорного эффекта алкильных групп.
В безводных минеральных кислотах карбоновые кислоты протонируются по кислороду с образованием карбкатионов:

Сдвиг электронной плотности в молекуле недиссоциированной карбоновой кислоты, о котором говорилось выше, понижает электронную плотность на гидроксильном атоме кислорода и повышает ее на карбонильном. Этот сдвиг еще больше увеличивается в анионе кислоты:

Результатом сдвига является полное выравнивание зарядов в анионе, который фактически существует в форме А - резонанс карбоксилат-аниона.
Первые четыре представителя ряда карбоновых кислот - подвижные жидкости, смешивающиеся с водой во всех отношениях. Кислоты, в молекуле которых содержится от пяти до девяти атомов углерода (а также изомасляная кислота), - маслянистые жидкости, растворимость их в воде невелика.
Высшие кислоты (от С 10) - твердые тела, практически нерастворимы в воде, при перегонке в обычных условиях они разлагаются.
Муравьиная, уксусная и пропионовая кислоты имеют острый запах; средние члены ряда обладают неприятным запахом, высшие кислоты запаха не имеют.

На физических свойствах карбоновых кислот сказывается значительная степень ассоциации вследствие образования водородных связей. Кислоты образуют прочные водородные связи, так как связи О-Н в них сильно поляризованы. Кроме того, карбоновые кислоты способны образовывать водородные связи с участием атома кислорода карбонильного диполя, обладающего значительной электроотрицательностью. Действительно, в твердом и жидком состоянии карбоновые кислоты существуют в основном в виде циклических димеров:
Такие димерные структуры сохраняются в некоторой степени даже в газообразном состоянии и в разбавленных растворах в неполярных растворителях.
